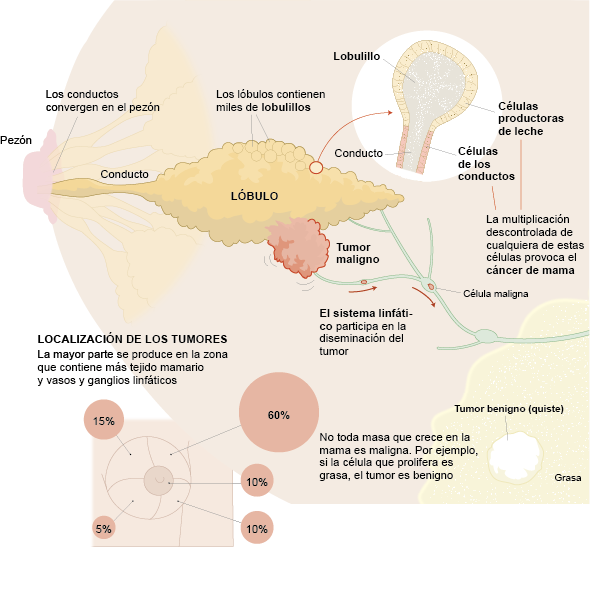
Cancer du sein
« La survie au cancer du sein a augmenté grâce aux progrès réalisés dans le diagnostic précoce et dans les thérapies appliquées contre cette pathologie. »
DR. ISABEL RUBIO RODRÍGUEZ
COORDINATEUR. DOMAINE DU CANCER DU SEIN

Qu’est-ce que le cancer du sein ?
Le cancer du sein est une maladie de la glande mammaire qui survient lorsque les cellules se multiplient et croissent de manière anormale. En conséquence, elles prolifèrent de façon incontrôlée et forment une tumeur. Il s’agit du cancer le plus fréquent chez la femme, bien qu’il puisse également toucher les hommes.
À la Clínica Universidad de Navarra, toute patiente présentant un symptôme est examinée par l’un de nos experts et bénéficie d’un plan de traitement personnalisé qui peut commencer une semaine seulement après la fin des examens diagnostiques.
L’Aire du Cancer du Sein de la Clinique Universidad de Navarra dispose des technologies les plus avancées pour le diagnostic et le traitement du cancer du sein. Environ 90 à 95 % des cancers du sein apparaissent de manière sporadique, c’est-à-dire qu’ils résultent d’altérations génétiques et d’autres facteurs de risque, sans pour autant être hérités.
Environ 5 à 10 % des cas de cancer du sein sont héréditaires. Cela signifie qu’ils sont dus à une altération (mutation) d’un gène pouvant avoir été transmise par le père ou la mère. À la Clinique, nous réalisons les examens nécessaires pour déterminer si votre cancer est sporadique (sans lien héréditaire) ou s’il est lié à une prédisposition génétique.
Si cela s’avère nécessaire, vous serez reçue en consultation à l’Unité de Médecine Génomique, où des spécialistes en conseil génétique vous expliqueront de manière claire et détaillée tout ce qui concerne ces gènes et leur signification pour vous et votre famille.
Contactez-nous et nous vous aiderons à trouver la meilleure solution

Symptômes du cancer du sein
Il est essentiel de consulter un spécialiste des pathologies mammaires si vous remarquez l’un des symptômes suivants :
- Une masse ou une zone épaissie dans le sein ou sous l’aisselle (au niveau de l’aisselle).
- Des changements dans la taille, la forme ou l’apparence du sein : toute asymétrie ou altération inhabituelle doit être examinée.
- Rétraction, eczéma ou affaissement du mamelon : ces modifications peuvent être liées à des affections sous-jacentes graves.
- Écoulement de sang ou d’un autre liquide par le mamelon : bien que cela n’indique pas toujours un cancer, ce symptôme doit être évalué.
- Changements cutanés, tels que rougeur, desquamation ou une texture rappelant la peau d’orange.
- Douleur persistante dans le sein : bien que la douleur mammaire soit souvent liée à des affections bénignes, elle peut également être un signe de cancer du sein.
- Inflammation partielle ou totale du sein, même sans présence de masse visible.
Rappelez-vous que la détection précoce est essentielle pour un traitement efficace du cancer du sein. En cas de changement suspect, consultez un médecin sans délai.
Présentez-vous l’un de ces symptômes ?
Si vous soupçonnez présenter l’un des symptômes mentionnés,
vous devez consulter un spécialiste pour établir un diagnostic.
Quelles en sont les causes ?
Les causes du cancer du sein sont multifactorielle : elles ne peuvent être attribuées à un seul facteur. Parmi ceux-ci figurent :
- Âge : le risque augmente avec l’âge. L’incidence la plus élevée du cancer du sein se situe entre 50 et 60 ans.
- Antécédents familiaux de cancer du sein : selon le nombre de membres de la famille concernés, leur degré de parenté (premier ou deuxième degré) et l’âge d’apparition, le risque de développer la maladie varie.
- Facteurs héréditaires : environ 5 à 10 % des cas sont héréditaires. La moitié d’entre eux sont liés à des mutations de deux gènes : BRCA1 et BRCA2. Dans ces situations, il est recommandé d’effectuer une étude génétique.
- Première grossesse après 30 ans ou absence de grossesse.
- Premières règles précoces (avant 12 ans) et ménopause tardive (après 55 ans).
- Certaines lésions bénignes du sein, notamment les lésions prolifératives avec atypies.
- Mode de vie : consommation d’alcool, obésité, tabagisme et sédentarité.
Plus de la moitié des femmes atteintes d’un cancer du sein ne présentent aucun de ces facteurs de risque, et toutes les femmes ayant un ou plusieurs de ces facteurs ne développent pas forcément la maladie. C’est pourquoi les systèmes de détection précoce revêtent une importance particulière.
Quels sont les types de cancer du sein ?
Il existe plusieurs types de cancer du sein, classés selon leur origine (canalaire ou lobulaire), leur comportement (invasif ou non invasif) et leurs caractéristiques moléculaires (récepteurs hormonaux et protéines spécifiques).
95 % prennent naissance dans l’épithélium des canaux ou des lobules mammaires (le tissu qui tapisse l’intérieur des canaux transportant le lait). Selon leur localisation, ils peuvent être canalaires, lobulaires ou, lorsqu’ils touchent le complexe aréole-mamelon, on parle de la maladie de Paget.
Moins de 1 % ont une origine mésenchymateuse, c’est-à-dire qu’ils proviennent de tissus tels que le tissu conjonctif, vasculaire ou musculaire du sein. Ces cas sont appelés sarcomes, comme les tumeurs phyllodes malignes ou l’angiosarcome.
Les caractéristiques moléculaires de la tumeur sont déterminées à l’aide de biomarqueurs tels que les récepteurs aux œstrogènes, à la progestérone, Her2 ou Ki-67. Ces indicateurs permettent de sélectionner des traitements personnalisés, adaptés aux caractéristiques de la tumeur, du patient et à ses préférences.
La décision thérapeutique est toujours prise conjointement entre l’équipe médicale et le patient.
Le cancer du sein peut-il être hérité ?
Dans environ 15 à 20 % des cas de cancer du sein, on observe des antécédents familiaux de la maladie sans qu’une mutation génétique héritée ne soit identifiée. Dans ces situations, le risque est probablement lié à des facteurs génétiques encore inconnus combinés à d’autres facteurs de risque.
En revanche, le cancer du sein héréditaire est causé par une mutation génétique identifiable, les gènes BRCA1 et BRCA2 étant les plus fréquents. Ces mutations sont également associées à d’autres types de cancer et peuvent être transmises aux enfants avec une probabilité de 50 %.
Être porteur sain d’une mutation génétique ne signifie pas que l’on développera un cancer, mais le risque de le contracter est nettement plus élevé que chez les personnes ne présentant pas cette mutation.
Quel est mon risque de développer un cancer du sein ?
À la Clinique Universidad de Navarra, nous disposons d’une consultation d’évaluation du risque de cancer du sein où, après analyse des antécédents familiaux et personnels ainsi que des caractéristiques mammaires de la patiente, un programme informatique permet de déterminer approximativement le risque de cancer du sein et de recommander les examens radiologiques les plus adaptés pour un diagnostic précoce.
Si vous présentez une lésion mammaire augmentant le risque de cancer du sein, nos spécialistes vous expliqueront la meilleure façon d’assurer un suivi approprié.
Comment diagnostique-t-on le cancer du sein ?
L’un des facteurs clés de succès dans le traitement du cancer du sein est l’évaluation globale par l’ensemble des spécialistes impliqués dans le processus et la rapidité à définir la meilleure stratégie thérapeutique.
C’est pourquoi la Clinique Universidad de Navarra dispose d’une unité médicale spécifique pour le diagnostic et le traitement du cancer du sein, composée d’une équipe multidisciplinaire de professionnels spécialisés dans cette pathologie.
Votre prise en charge comprend un interrogatoire clinique, un examen physique et des examens d’imagerie tels que :
- Mammographie
- Échographie mammaire
- Imagerie par résonance magnétique ou mammographie de contraste
- Biopsie mammaire - à l’aiguille large ou sous vide
Comment traite-t-on le cancer du sein ?
Tumorectomie du sein
La tumorectomie ou chirurgie conservatrice du sein est le traitement chirurgical indiqué dans 70 à 80 % des cas de cancer du sein. Elle consiste à retirer uniquement la tumeur tout en conservant le reste du tissu mammaire. Il a été démontré qu’elle offre les mêmes résultats oncologiques que la mastectomie et qu’elle améliore la qualité de vie des patientes, selon de nombreuses études.
Dans la majorité des cas, une hospitalisation de 24 heures est suffisante, bien que, dans certaines situations, l’intervention puisse être réalisée en ambulatoire. Chaque fois que possible, on privilégie des cicatrices discrètes (au bord de l’aréole, dans le sillon sous-mammaire ou au niveau de l’aisselle) ou des techniques de chirurgie oncoplastique, combinant chirurgie oncologique et chirurgie plastique afin d’obtenir le meilleur résultat esthétique.
Ces techniques permettent de retirer la tumeur avec des marges de sécurité adéquates et de remodeler le sein pour un résultat esthétique optimal, réduisant ainsi la nécessité de mastectomies.
De plus, la survie après chirurgie conservatrice combinée à la radiothérapie est équivalente à celle obtenue après mastectomie.
À la Clinique Universidad de Navarra, nos chirurgiens sont des pionniers experts dans l’utilisation de l’échographie peropératoire, améliorant la précision chirurgicale pour les tumeurs non palpables et réduisant le risque de marges positives.
Mastectomie
Dans 20 à 30 % des cas, l’ablation complète du sein (mastectomie) est nécessaire. Plusieurs techniques peuvent être employées selon le cas clinique :
- Mastectomie simple : retrait de tout le tissu mammaire, y compris la peau et le complexe aréole-mamelon. Elle nécessite une hospitalisation de 1 à 2 jours et peut être combinée à d’autres traitements.
- Mastectomie radicale modifiée : retrait du tissu mammaire, du complexe aréole-mamelon et des ganglions lymphatiques axillaires. Elle requiert également 1 à 2 jours d’hospitalisation et peut inclure une reconstruction immédiate.
- Mastectomie avec préservation de la peau : la peau du sein est conservée, mais le complexe aréole-mamelon est retiré. Cette technique améliore le résultat esthétique de la reconstruction.
- Mastectomie avec préservation de la peau et du complexe aréole-mamelon : toute la peau ainsi que le complexe aréole-mamelon sont conservés, offrant un résultat plus naturel après la reconstruction. Pour la pratiquer, un examen préalable par mammographie, IRM et biopsie du mamelon est réalisé afin de confirmer l’absence d’atteinte tumorale.
À la Clinique Universidad de Navarra, nous effectuons la reconstruction mammaire dans 90 % des cas après mastectomie, garantissant une approche globale qui améliore la qualité de vie et les résultats esthétiques de nos patientes. Lorsque la patiente doit recevoir une radiothérapie après la mastectomie, nous évaluons également la reconstruction immédiate : jusqu’à 60 % des patientes concernées en bénéficient.
La radiothérapie postopératoire constitue une étape essentielle pour réduire le risque de récidive tumorale dans la zone opérée. Il est en effet démontré qu’elle diminue ce risque d’environ un tiers.
À la Clinique Universidad de Navarra, nous possédons une grande expérience en radiothérapie conventionnelle (irradiation de l’ensemble du sein pendant six semaines) ainsi qu’en radiothérapie partielle (irradiation uniquement de la zone où se trouvait la tumeur, appelée lit tumoral, pendant seulement cinq jours).
Dans les cas de cancers du sein à un stade initial, la radiothérapie partielle, ciblant uniquement la zone à plus haut risque, offre des résultats très satisfaisants, avec un risque de rechute minimal.
La Clinique Universidad de Navarra a mis en œuvre différentes techniques d’irradiation partielle du sein :
Curiethérapie mammaire à haut débit de dose peropératoire
- Procédure mini-invasive permettant d’administrer la radiothérapie directement dans le lit tumoral, pendant l’intervention chirurgicale d’exérèse.
- Réduit la durée du traitement de six semaines à seulement cinq jours.
- Une fois le traitement terminé, les cathéters sont retirés simplement en consultation, sans anesthésie.
- Nous sommes un centre de référence international et le plus expérimenté dans cette technique.
Curiethérapie mammaire à haut débit de dose peropératoire + radiothérapie externe avec technique « forward »
- Indiquée lorsque le cancer est plus étendu.
- Associe la curiethérapie sur la zone à plus haut risque à une radiothérapie externe sur le reste du tissu mammaire, afin d’assurer un traitement complet.
Radiothérapie externe avec technique « forward »
- Permet une administration plus homogène du rayonnement que la technique conventionnelle, réduisant ainsi les effets secondaires aigus.
- Raccourcit le traitement à 15 séances, contre 25 pour la radiothérapie traditionnelle.
Radiothérapie externe partielle avec technique accélérée
- Irradie uniquement le lit tumoral, sans traiter l’ensemble du sein.
- Nous utilisons un schéma accéléré de cinq jours, concentrant la dose totale sur une durée plus courte et évitant ainsi des traitements prolongés de plusieurs semaines.
Le choix du traitement chimiothérapique le plus approprié dépend de plusieurs facteurs :
- Taille de la tumeur.
- Atteinte des ganglions lymphatiques.
- Présence ou non de métastases à distance.
- Traitements préalablement reçus.
- Sous-type de cancer du sein (selon la présence de récepteurs aux œstrogènes, à la progestérone, HER2, etc.).
- Âge et état général de santé.
- Autres maladies associées (comorbidités).
- Effets secondaires potentiels du traitement.
En général, la chimiothérapie dans le cancer du sein peut être administrée dans trois contextes :
Adjuvante (après la chirurgie)
- Utilisée dans les tumeurs localisées afin de renforcer le traitement local.
- Son objectif est d’éliminer les cellules tumorales circulantes ou les micrométastases non détectées, réduisant ainsi le risque de rechute.
Néoadjuvante (avant la chirurgie)
- Permet d’instaurer plus tôt le traitement systémique.
- Aide à évaluer la réponse de la tumeur à la chimiothérapie (réduction de sa taille).
- Peut diminuer le volume tumoral, facilitant ainsi une chirurgie plus conservatrice ou rendant opérables des tumeurs initialement inopérables.
Dans les formes avancées ou métastatiques
- Elle est employée pour contrôler les métastases et freiner la progression de la maladie, tout en améliorant la qualité de vie.
À la Clinique Universidad de Navarra, nous disposons de protocoles spécifiques et d’une grande expérience dans l’administration de la chimiothérapie chez les femmes enceintes atteintes d’un cancer du sein, en garantissant toujours la sécurité maximale pour la mère et le bébé.
Nous disposons d’un large choix de médicaments chimiothérapiques permettant d’adapter le traitement à chaque type de tumeur et à chaque situation clinique.
Le traitement hormonal, également appelé thérapie endocrinienne, constitue une stratégie essentielle pour traiter les tumeurs du sein présentant des récepteurs hormonaux positifs (HR+), c’est-à-dire celles qui se développent sous l’effet des hormones comme l’œstrogène (ER) et/ou la progestérone (PR).
Ce type de tumeur est le plus fréquent : il représente entre 70 % et 80 % de l’ensemble des cancers du sein.
Au cours des dernières années, le traitement hormonal du cancer du sein hormonosensible (HR+) a connu des progrès considérables, tant aux stades précoces que dans les formes avancées, grâce à de nouveaux médicaments et à une approche plus personnalisée en fonction des caractéristiques biologiques de la tumeur.
Il est démontré que la thérapie hormonale réduit le risque de rechute et améliore la survie des patientes atteintes de ce type de cancer.
Modulateurs sélectifs des récepteurs aux œstrogènes (SERM)
- Exemple : Tamoxifène.
- Bloque l’action des œstrogènes sur les cellules tumorales, empêchant leur croissance.
Inhibiteurs de l’aromatase
- Exemples : Anastrozole, Létrozole, Exemestane.
- Réduisent la quantité d’œstrogènes produite par l’organisme, limitant ainsi la stimulation hormonale de la tumeur.
Analogues de la LHRH (hormone de libération des gonadotrophines)
- Exemples : Goséréline, Triptoréline.
- Bloque la production d’œstrogènes par les ovaires, particulièrement utile chez les femmes préménopausées.
SERD (Selective Estrogen Receptor Degraders ou dégradeurs sélectifs du récepteur aux œstrogènes)
- Exemples : Fulvestrant, Camizestrant, Elacestrant.
- Ces médicaments ne se contentent pas de bloquer l’action des œstrogènes, ils détruisent également le récepteur aux œstrogènes dans la cellule tumorale.
- Actuellement approuvés pour le cancer du sein avancé ou métastatique, ils sont également à l’étude pour les stades précoces.
Autres médicaments associés : inhibiteurs de CDK4/6
- Exemples : Palbociclib, Ribociclib, Abemaciclib.
- Utilisés pour les tumeurs présentant des récepteurs hormonaux positifs et HER2 négatif, dans les formes avancées ou métastatiques.
- Les protéines CDK4 et CDK6 régulent le cycle cellulaire, c’est-à-dire le processus par lequel les cellules croissent et se divisent.
- Ces médicaments bloquent cette division cellulaire et sont généralement administrés en association avec une thérapie hormonale telle que le létrozole, l’anastrozole, le fulvestrant ou le tamoxifène.
- Ils représentent une avancée majeure dans le traitement, prolongeant le contrôle de la maladie.
Le système immunitaire joue un rôle essentiel dans la défense contre le cancer. L’immunothérapie vise à stimuler ou « réentraîner » les défenses naturelles de la patiente afin que son propre organisme reconnaisse et détruise les cellules tumorales.
Dans le cancer du sein, l’immunothérapie a pris une importance croissante, en particulier dans les sous-types agressifs tels que le cancer du sein triple négatif (TNBC), qui ne présente pas de récepteurs hormonaux ni HER2 et pour lequel les options de traitement conventionnelles sont plus limitées.
Comment cela fonctionne
L’une des stratégies les plus utilisées repose sur les inhibiteurs des points de contrôle immunologiques (anticorps anti-PD-1 et anti-PD-L1).
- Ces médicaments « retirent les freins » du système immunitaire, permettant aux défenses de mieux attaquer la tumeur.
- Associés à la chimiothérapie, ils ont montré une amélioration de la survie et du contrôle de la maladie chez les patientes atteintes d’un cancer du sein avancé ou métastatique.
Vaccins personnalisés contre le cancer du sein
À la Clinique Universidad de Navarra, des vaccins individualisés sont également utilisés dans le cadre de protocoles d’immunothérapie :
- Ils sont fabriqués à partir des propres cellules de la patiente (vaccins autologues), ce qui évite tout risque de rejet.
- Les antigènes (marqueurs uniques) de la tumeur sont isolés afin que le système immunitaire puisse les identifier et les attaquer.
- Ils sont administrés en association avec la chimiothérapie, notamment dans les formes localisées nécessitant ce traitement.
Avantages
- Bonne tolérance, car il s’agit d’un produit issu du propre organisme de la patiente.
- Traitement personnalisé et compatible avec la chimiothérapie.
- Peut être poursuivi sur une longue période, notamment pendant les cinq premières années suivant le diagnostic, lorsque le risque de rechute est le plus élevé.
Comment ils sont produits
- Les cellules sont prélevées sur la patiente puis traitées dans le laboratoire GMP de thérapie cellulaire de la Clinique.
- Les antigènes tumoraux obtenus à partir de ces cellules sont incorporés au vaccin.
- Le traitement est administré selon un calendrier vaccinal de deux ans, en complément du traitement oncologique standard.
Recherche et utilisation actuelle
La Clinique a réalisé un essai clinique visant à évaluer l’efficacité de ces vaccins dans un sous-groupe de cancers du sein ne présentant pas d’expression de la protéine HER2.
Actuellement, ils sont proposés comme traitement compassionnel afin de compléter les thérapies habituelles.
Dans certains cas de cancer du sein, les cellules tumorales produisent en excès une protéine appelée HER2 (récepteur 2 du facteur de croissance épidermique humain). Cette protéine stimule la croissance de la tumeur de façon plus rapide et plus agressive.
Environ 10 % à 20 % des cancers du sein présentent cette surexpression de HER2.
Pour ce type de tumeurs, il existe des traitements spécifiques par inhibiteurs du récepteur HER2, qui se sont révélés très efficaces lorsqu’ils sont associés à la chimiothérapie, permettant :
- Une meilleure réponse de la tumeur au traitement.
- Une prolongation de la survie.
À la Clinique Universidad de Navarra, nous poursuivons nos recherches sur de nouvelles thérapies afin d’améliorer leur efficacité et de réduire les effets secondaires de ces traitements.
Anticorps conjugués à des médicaments (ADC)
Les ADC (Antibody-Drug Conjugates, ou anticorps conjugués à un médicament) représentent l’une des stratégies les plus innovantes dans le traitement du cancer du sein, en particulier pour les tumeurs HER2 positives ou triples négatives.
Mode d’action :
- Ils associent un anticorps monoclonal (qui reconnaît une protéine spécifique de la cellule tumorale, comme HER2 ou Trop-2) à un médicament chimiothérapique très puissant.
- L’anticorps agit comme un « missile guidé », se liant uniquement aux cellules cancéreuses exprimant cette protéine.
- Une fois lié, il libère le médicament directement à l’intérieur de la tumeur, détruisant les cellules malignes tout en épargnant les tissus sains.
Avantages :
- Précision accrue dans l’attaque ciblée de la tumeur.
- Toxicité générale inférieure à celle de la chimiothérapie classique.
- Amélioration démontrée de la survie et de la qualité de vie chez les patientes atteintes de cancer du sein avancé ou métastatique.
Actuellement, plusieurs ADC sont déjà approuvés pour le traitement du cancer du sein, et de nombreux autres font l’objet d’essais cliniques avancés.

UNE MÉDECINE PERSONNALISÉE
Deuxième avis,
la tranquillité de savoir
Demandez un deuxième avis à nos professionnels ayant une grande expérience dans le diagnostic et le traitement des maladies oncologiques.
En 3 jours, sans sortir de chez vous.
Ou, si vous le préférez, vous pouvez vous rendre à la Clinique.
Pourquoi choisir la Clinique Universidad de Navarra ?
LES TRAITEMENTS LES PLUS AVANCÉS
Chirurgie oncoplastique et
reconstruction mammaire
Nos chirurgiens sont spécialisés dans la planification chirurgicale visant à préserver la plus grande quantité possible de tissu mammaire sain et, si nécessaire, à procéder à une reconstruction mammaire immédiate.
- Chirurgie oncoplastique conservatrice.
- Mastectomie avec conservation de l’aréole et du mamelon.
- Échographie peropératoire.
- Préservation des ganglions axillaires.
- Reconstruction mammaire immédiate.
Thérapies ciblées et immunothérapie contre le cancer du sein
Nous disposons d’une vaste expérience dans l’administration des thérapies les plus innovantes, telles que les vaccins dendritiques, qui complètent le traitement standard.
- Traitements basés sur l’immunothérapie.
- Vaccins contre le cancer du sein.
Irradiation partielle
accélérée
Pionniers en Espagne dans l’irradiation partielle accélérée par curiethérapie, nous réduisons la durée de la radiothérapie à cinq jours au lieu des vingt-cinq habituels.
- Curiethérapie interstitielle.
- Curiethérapie peropératoire.
- Radiothérapie peropératoire.
- Techniques innovantes de radiothérapie (thérapie par protons).
Protonthérapie contre le cancer
La thérapie par protons est la modalité de radiothérapie externe la plus précise, offrant une meilleure répartition de la dose de rayonnement et donc une irradiation moindre des tissus sains.
L’Unité de protonthérapie ou de thérapie par protons du Cancer Center Clínica Universidad de Navarra, située à Madrid, est la plus avancée d’Europe et la première intégrée dans un centre de cancérologie, bénéficiant de tout le soutien clinique, académique et de recherche de l’institution.
Quels essais cliniques avons-nous sur Cancer du sein?
Notre équipe de professionnels
Nous aidons nos patients à surmonter leur passé
Vos témoignages nous encouragent à continuer d'améliorer nos services